Selpercatinib rappresenta lo standard di seconda linea, approvato dall’Agenzia Italiana del Farmaco (AIFA), nei pazienti con non-small cell lung cancer (NSCLC) e fusione di RET. Il trial di fase III LIBRETTO-431 ha randomizzato 212 pazienti a ricevere selpercatinib vs chemioterapia a base di platino ± pembrolizumab in prima linea di trattamento. Il cross-over era consentito. Endpoint primario: progression-free survival (PFS) mediana.
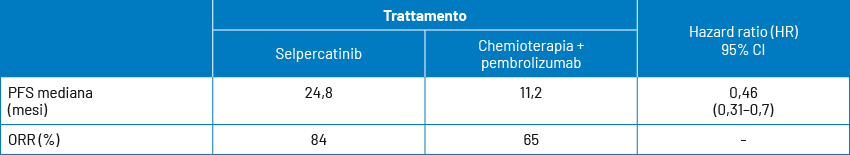
Il netto beneficio dimostrato da selpercatinib porterà all’approvazione anche in prima linea per i pazienti con NSCLC avanzato e fusione di RET. Il trattamento ha dimostrato un’ottima azione anche a livello del sistema nervoso centrale (hazard ratio, HR 0,28; confidence interval, CI 95%: 0,12–0,68). Il profilo di safety (G3) è stato caratterizzato prevalentemente da rialzo delle aspartato aminotransferasi/alanina aminotransferasi (AST/ALT, 22%) e ipertensione arteriosa (20%).